全球约 3990 万人受 HIV-1 感染,现有联合抗逆转录病毒治疗(cART)虽能有效抑制病毒复制、控制病情进展,却无法根除体内潜伏病毒库,患者需终身服药维持,一旦停药即出现病毒反弹,功能性治愈仍是全球抗艾领域的核心难题。近日,清华大学药学院廖学斌教授团队、医学院张林琦教授团队与森妙生物联合攻关,在《Journal of Medicinal Chemistry》发表重磅研究成果,成功研发出高选择性 TLR8 激动剂 23a(SV-128),该化合物凭借独特的双重作用机制与优异的药学特性,为 HIV“shock and kill” 治疗策略提供了全新解决方案,有望推动 HIV 功能性治愈研究迈入新阶段。
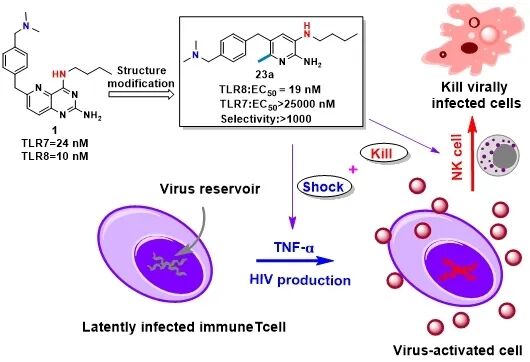
精准靶向 TLR8,攻克选择性与活性双重瓶颈
TLR7/8 作为识别病原体单链 RNA 的模式识别受体,其激活可启动先天免疫反应,成为 HIV 潜伏库激活的关键靶点。但此前 TLR7 激动剂(GS-9620)存在免疫激活效力不足、疗效有限等问题,而 TLR8 特异性激动剂的研发因结构优化难度大,始终进展缓慢。该团队通过结构导向药物设计,融合杂交策略与代谢优化,获得兼具高活性与高选择性的新型化合物。23a 的 TLR8 激动活性达 19 nM,对 TLR7 的选择性高于 1300 倍,显著优于TLR8激动剂 GS-9688(选择性低于100倍)和VTX-2337(选择性低于50倍)。
分子对接技术揭示了其高选择性的结构基础:23a 可与 TLR8 的 Thr586 残基形成特异性氢键,而 TLR7 中对应的 Thr574 残基构象向外,无法形成该相互作用,从而避免了交叉激活引发的免疫紊乱风险。同时,23a 的 N1 原子 pKa 值达 9.41,较对照化合物11a提升 1.57,增强了与 TLR8 关键残基 Asp543 的离子氢键作用,进一步提升了激动活性。
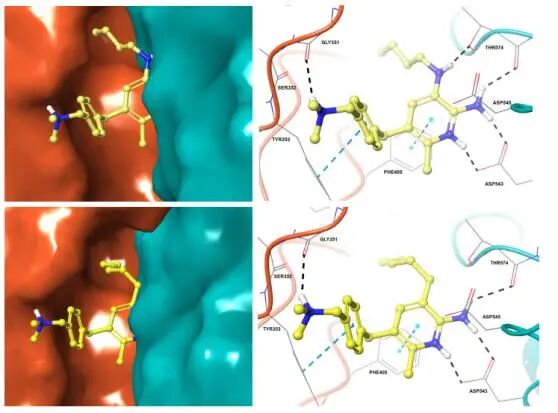
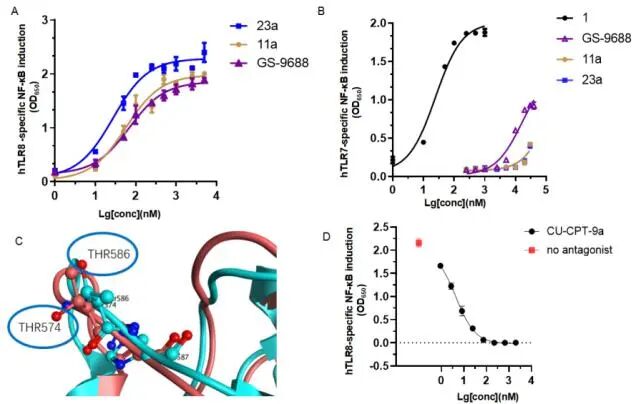
图1 TLR8激动剂23a与TLR8蛋白的分子结合模式,及其激动活性和选择性
双重机制协同,实现 “激活 - 清除” 闭环
23a 的核心优势在于完美契合 “shock and kill” 策略的双重需求,在体外实验中展现出远超现有候选药物的综合效能。
在 “shock” 潜伏病毒库方面,23a 以浓度依赖方式强效激活 HIV-1 感染的单核细胞系(U1)、T 淋巴细胞系(ACH-2)及早幼粒细胞系(OM10.1)中的潜伏病毒,显著提升细胞上清中 p24 抗原水平,激活效果优于临床研究用 TLR7 激动剂 GS-9620 和 TLR8 激动剂 GS-9688。更关键的是,在接受长期 cART 治疗的 HIV 患者外周血单个核细胞(PBMCs)中,23a 能有效诱导潜伏病毒重新转录,使原本近乎检测不到的 HIV RNA 水平显著升高,证实了其对临床艾滋病人样本同样具有激活潜伏病毒的作用。
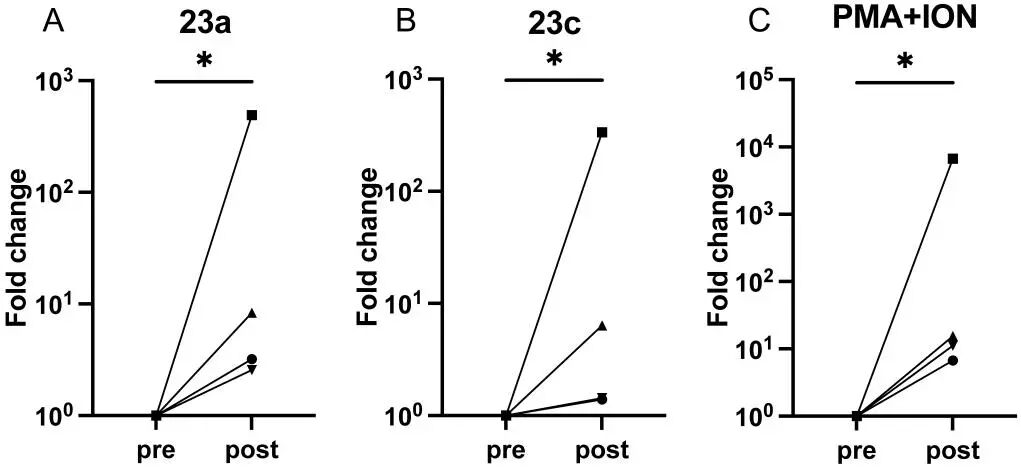
图2 TLR8激动剂23a和23c激活艾滋病患者的潜伏病毒库
在 “Kill” 感染细胞方面,23a 可有效激活先天免疫中的自然杀伤(NK)细胞,使其高表达活化标志物 CD69,并大量分泌干扰素 -γ(IFN-γ)。激活后的 NK 细胞能精准识别并清除 HIV 感染的 CD4+ T 细胞,同时诱导患者 PBMCs 产生 TNF-α、IL-12等细胞因子,进一步放大免疫清除效应,形成对感染细胞的 “围剿” 闭环。
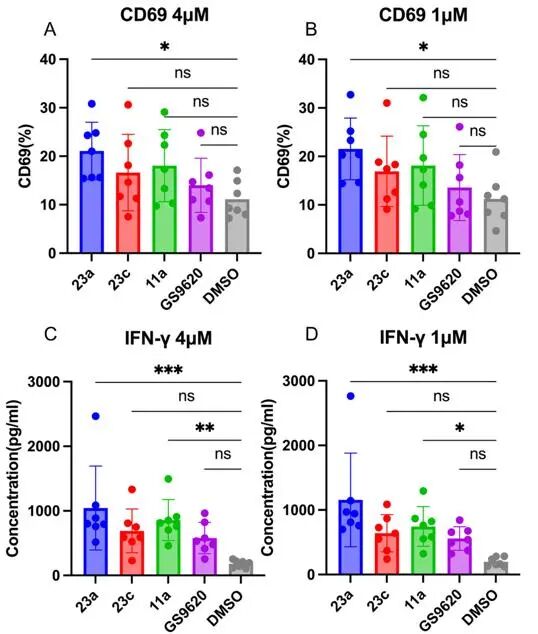
图3 TLR8激动剂23a激活NK 细胞,并释放IFN-γ
联合治疗潜力巨大,引领治愈研究新方向
该研究的核心突破在于首次开发出兼具高活性、高选择性和良好药代动力学性质的 TLR8 选择性激动剂,其不仅能高效激活潜伏病毒库,还能直接激活免疫效应细胞,突破了传统潜伏逆转剂仅能单一激活病毒、依赖额外免疫手段清除的局限。
研究团队表示,未来可探索将 23a 与治疗性疫苗、广谱中和抗体、免疫检查点抑制剂等疗法联合使用,进一步提升 HIV 病毒库的清除效率。目前,团队正推进该化合物的临床前深入研究,计划在非人灵长类动物模型中评估其体内病毒清除效果,为后续临床转化奠定基础。
致谢
该研究由清华药学廖学斌教授和清华医学张林琦教授为共同通讯作者;药学院已毕业博士生王志松博士(现为森妙生物首席技术官)、医学院已毕业博士生李杨阳博士为共同第一作者。研究得到森妙生物王杰博士,药学院已毕业博士生孙淑豪博士、已出站博士后张逸轩博士的大力支持。本研究得到清华-北京生命科学中心传染病诊疗协同创新中心、罗氏博士后基金项目以及国家自然科学基金青年基金项目(82402704,Y.L.)的支持。
科学家小档案

廖学斌 清华大学药学院
1995年毕业于北京大学化学与分子工程学院,1998-2004年期间在威斯康星大学密尔沃基分校(University of Wisconsin-Milwaukee)获得有机化学博士学位;2005-2008年期间随世界著名化学家 John F. Hartwig先后在耶鲁大学以及伊利诺伊大学香槟分校从事博士后研究;2009年至2012年在诺华功能基因组研究院(GNF)以高级研究员(PI)的身份开展药学研究。2012年9月正式加入清华大学,研究员、博士生导师。廖学斌博士于2013-2015年获得了“Tsinghua-Janssen Investigator”awards,2018年获“Roche Chinese Investigator Award”, 2020年获“The Thieme Chemistry Journals Award”。