近日,清华大学基础医学院郭晓欢团队在Gut Microbes期刊发表了题为“The gut microbiota and host immunity synergistically orchestrate colonization resistance”的综述文章,系统总结了肠道定植抵抗(colonization resistance)的分子机制及其在肠道感染中的研究进展。

肠道定植抵抗是宿主抵御肠道病原体定植和感染的重要防线,其建立依赖于肠道微生物群与宿主免疫系统之间的高度协同。该综述从微生物与宿主两个层面,系统梳理了定植抵抗的多层次调控机制。
在微生物层面,共生菌群通过生态位与营养竞争、接触依赖性抑制机制以及抗菌化合物和代谢产物的产生,直接限制肠道病原体的生存和扩增。在宿主层面,肠道上皮屏障、天然与获得性性免疫应答以及抗菌肽的精细调控,在维持肠道微生态稳态的同时,对病原体形成选择性限制。
值得关注的是,文章重点强调了ILC3-IL-22信号通路在定植抵抗中的关键作用。IL-22 通过调控肠上皮细胞糖基化模式(岩藻糖基化、半乳糖基化等),改变肠道内营养物可利用性,从而塑造微生物竞争格局并增强宿主对病原体的抵抗能力。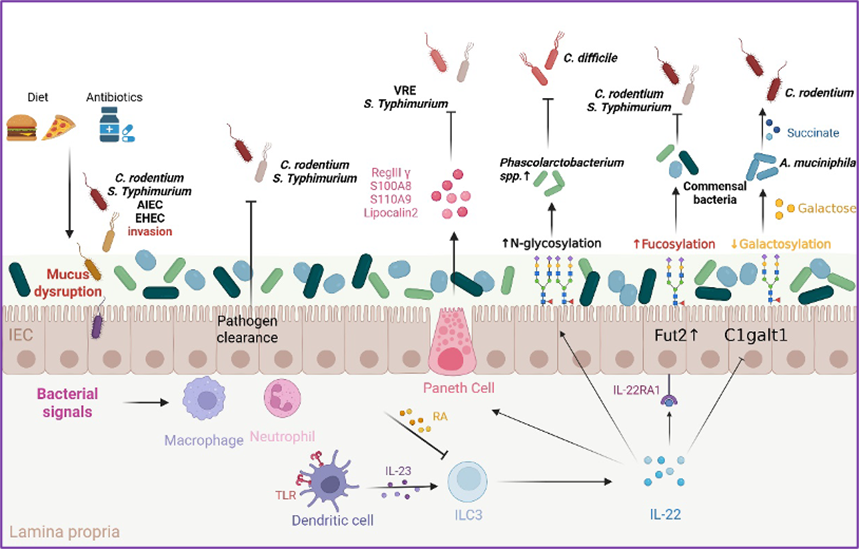
肠道定植抵抗并非单一因素的结果,而是微生物生态与宿主免疫长期协同进化形成的综合防御体系。深入理解这一过程,将为感染性疾病和炎症性肠病的防治提供新的干预思路。该综述还讨论了定植抵抗研究面临的挑战及未来发展方向,指出整合微生物组学、免疫学和代谢研究,将有助于推动新型抗感染策略和微生态干预手段的转化应用。
清华大学基础医学院郭晓欢副教授为本文的通讯作者,清华大学基础医学院博士生李娜为本文的第一作者。课题组长期聚焦于以ILC3s为核心的黏膜免疫调控研究,近年内陆续解析了ILC3s维持黏膜免疫耐受与菌群稳态的多种新机制(Nat Microbiol 2025,J Exp Med 2024等),发现了ILC3s等在黏膜感染、炎症、肿瘤等疾病中发挥的关键作用与调控机制(Sci Immunol 2025, Cell Metab 2021, Nat Commun 2024, Mucosal Immunol 2024, J Allergy Clin Immunol 2022等),推动了相关领域的发展,被国际黏膜免疫学学会会刊遴选为“Emerging leader in mucosal immunology”。本课题获得了国家自然科学基金、国家重点研发计划、山西医科大学-清华大学前沿医学协同创新中心等项目的支持。
文章链接
https://www.tandfonline.com/doi/full/10.1080/19490976.2025.2611545