对心脏病患者而言,植入式心脏起搏器是恢复正常心律的“救命神器”。植入式生物电子设备凭借精准调控细胞活动的能力,不仅能修复心律功能,还广泛应用于运动、视听功能恢复、疼痛管理及疾病诊断等领域,为重大疾病的早期干预、精准治疗和长期管理提供关键支撑,显著改善患者生活质量并减轻家庭照护负担。然而,设备电池耗尽后需二次手术更换,成为一大难题。相比首次植入,二次手术创伤更大、风险更高,且带来沉重经济负担。因此,“终身免维护运行”成为该领域的终极目标,而实现这一目标的关键,在于突破终身供能的技术瓶颈。
理念创新
从“被动耗能”到“主动供电”
为破解这一难题,清华大学生物医学工程学院李舟团队跳出传统设备设计思路,突破电子器件必须由电池或无线供电的固有认知,提出通过人体自供电的方式实现植入式电子设备的能源供给。研究团队于2014年研制了首款自供电心脏起搏器(Advanced Materials, 2014, 26(33):5851-5856),2019年成功研制出共生型自供电心脏起搏器,相关成果发表于《自然·通讯》(Nature Communications, 2019,10,1821)并提出“共生生物电子(symbiotic bioelectronics)”创新理念。此后,团队持续拓展该自供电生物电子器件的应用边界,在骨修复、神经调控及生物可吸收电子器件等领域接连取得重要进展( Nature Communications, 2024, 15:507; Science Advances,2024, eadi6799; Device,2025,3, 100724; Advanced Science,2024,2410289)。
技术突破
联合攻关打造“人机共生”自供电微型起搏器
历经近七年联合攻关,李舟及其合作者中国医学科学院阜外医院华伟教授、中国科学院大学欧阳涵副教授等组成的研究团队,终于取得重要进展——成功研发出胶囊尺寸的微型共生型自供电无导线心脏起搏器。相关研究成果以“共生型经导管起搏器在疾病模型中实现终身能量再生与治疗功能”(Symbiotic transcatheter pacemaker for lifelong energy regeneration and therapeutic function in porcine disease model)为题,于2026年1月19日在《自然生物医学工程》(Nature Biomedical Engineering)上发表。

这款起搏器的核心创新是集成了高效能量再生模块:它能通过电磁感应技术,从心脏自身的跳动中捕获动能,并将其转化为电能。测试显示,其输出功率已突破起搏器终身运行的临界能量阈值,可稳定驱动起搏电路,实现对心脏节律的精准调控。同时,器件采用高度微型化设计,兼具优异的生物相容性与血液相容性,支持经导管微创植入,大幅降低手术创伤。团队创新设计的极简磁悬浮能量缓存结构,不仅最大限度减少了能量损耗和机械摩擦,还实现了近零启动阈值、高动能转换效率及稳定的心内平均输出功率,同时简化系统复杂度,提升了设备的长效稳定性。
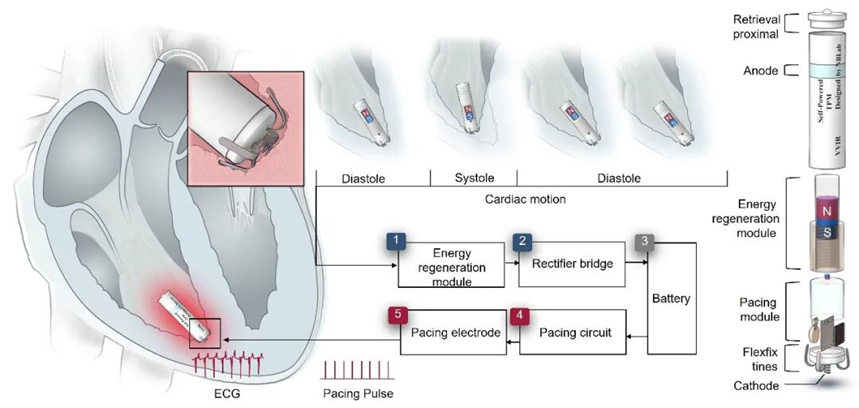
共生型自供电无导线心脏起搏器示意图
临床前评估
一个月长效动物实验测试转化潜力
在猪三度房室传导阻滞心律失常模型中,该共生型起搏器完成了为期一个月的自主运行测试。实验期间,它持续实现能量自供给,同时稳定发挥起搏治疗功能,有效调控实验动物的心脏节律,充分验证了其临床转化可行性。
这一技术突破有望将起搏器的使用寿命延长至与自然心脏一致的水平,彻底解决二次手术的痛点,为植入式电子器件实现真正意义上的“终身免维护”和“人机共生”开辟了全新路径。
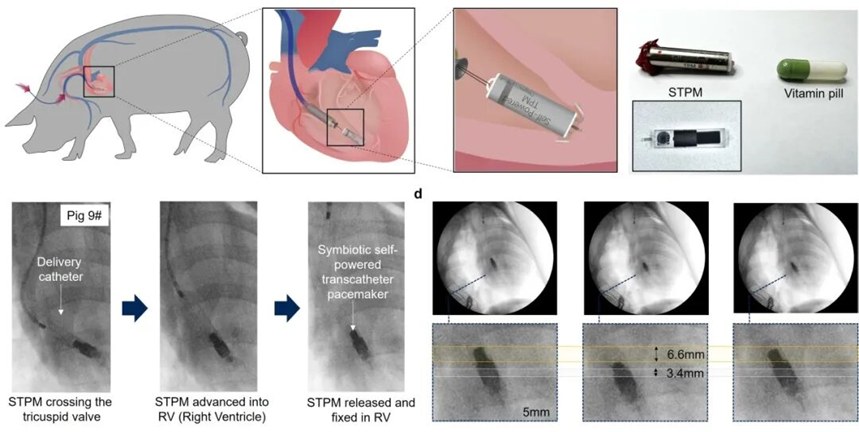
体内植入过程示意图与DR影像
清华大学生物医学工程学院、北京清华长庚医院李舟研究员与中国医学科学院阜外医院华伟教授为本文通讯作者,中国科学院大学欧阳涵副教授、北京大学/北医三院蒋东杰副研究员、中国医学科学院阜外医院胡奕然博士与程思静博士、杭州电子科技大学张正民副教授为论文第一作者。
中国科学院北京纳米能源与系统研究所王中林院士对该工作给予了重要支持。该工作得到了国家自然科学基金、国家重点研发计划、中科院青年创新促进会、北京市自然科学基金、北京市科技新星计划、新曦颠覆性技术创新基金以及中央高校基本科研业务费专项资金的联合资助。