肠道中存在一种“潜伏”病毒——原噬菌体(Prophage)。它们是温和噬菌体整合入细菌基因组后的形式,能够随宿主细菌一起复制。研究表明,原噬菌体在人体和小鼠肠道中广泛存在,尤其在婴儿粪便中,超过80%的分离菌株携带能够释放噬菌体颗粒的原噬菌体。尽管数量丰富,其在人体肠道生态系统中的作用尚未被系统解析。
2025年12月30日,清华大学基础医学院梁冠翔课题组与中国科学院分子细胞科学卓越创新中心宋昕阳课题组合作在《Nature Communications》上发表题为“Human gut prophage landscape identifies a prophage-mediated fucosylation mechanism alleviating colitis”的研究论文。该研究系统绘制了人体肠道原噬菌体图谱,揭示了其在不同健康状态和疾病状态下的分布特征,并发现原噬菌体通过岩藻糖基化调控肠道屏障功能,从而对结肠炎发挥保护作用。
该研究设计了一套原噬菌体识别分析流程,对UHGG数据库中289,232个人类肠道微生物基因组进行了系统分析。结果显示,原噬菌体在肠道细菌中广泛存在,但不同类别细菌间的分布存在显著差异。同时,分类学和功能注释分析进一步扩展了原噬菌体的分类学和功能多样性(图1)。
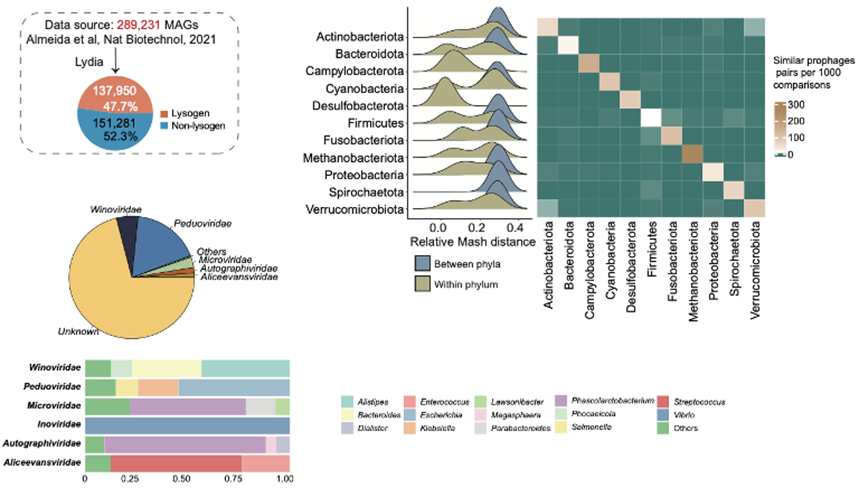
图1. 人体肠道原噬菌体的分类及分布特征
进一步对8503份肠道宏基因组样本的分析表明,携带原噬菌体的溶原细胞比例在不同人群间差异显著,并与年龄、健康状况及地理分布(尤其是工业化水平)密切相关(图2)。

图2. 原噬菌体与人体特征的关联分析
更为关键的是,原噬菌体编码的功能基因在疾病状态下表现出特异性变化。特别是在炎症性肠病患者中,编码α-1,2-岩藻糖基转移酶基因(futC)的原噬菌体显著减少。体外实验表明,该酶可驱动2'-fucosyllactose(2'-FL)的生物合成;进一步的动物实验显示,2'-FL可减轻DSS诱导的小鼠结肠炎,其机制包括通过肠道微生物促进IgA分泌和上皮CD4⁺CD8αα⁺ T细胞发育,从而增强肠道黏膜屏障功能(图3)。这一发现提示原噬菌体可能通过编码功能基因调控宿主免疫和上皮屏障,从而影响肠道稳态。

图3. 2'-FL调控肠道免疫缓解结肠炎
清华大学基础医学院梁冠翔助理教授和中国科学院分子细胞卓越创新中心宋昕阳研究员为本文通讯作者;清华大学基础医学院已毕业博士生高鸿雁和中国科学院分子细胞卓越中心博士生王亚婷为共同第一作者。清华大学罗赛助理教授、姚骏副教授、白净卫研究员以及基础医学院博士生赵雨林、焦宪悦、郭子菡、郑磊、李一琛等也为本研究做出了重要贡献。基础医学院刘锦涛副教授与张敬仁教授也提供了重要帮助。研究得到国家自然科学基金、科技部重点研发计划、清华-北大生命科学联合中心、清华大学启动基金、清华大学笃实基金、山西医科大学-清华大学医学院前沿医学协同创新基金及中国科学院战略性先导科技专项等项目资助。
文章链接
https://www.nature.com/articles/s41467-025-66733-5