2021年10月25日,清华大学医学院、清华大学免疫学研究所胡小玉课题组在《Mucosal Immunology》(黏膜免疫)杂志在线发表了题为“Epithelial NELF guards intestinal barrier function to ameliorate colitis by maintaining junctional integrity”(上皮细胞转录延伸因子复合物通过维持肠道上皮细胞屏障功能完整性来改善结肠炎)的研究论文,揭示了转录延伸负调控因子NELF复合物(negative elongation factor complex)通过调控细胞连接基因表达和抑制上皮细胞坏死来维持肠道上皮细胞屏障功能完整性,从而减缓结肠炎发病进程。
上皮组织是哺乳动物隔离外界环境的第一道防线,而由肠道上皮细胞构成的肠道黏膜屏障可以帮助机体把肠腔环境中的病原体或共生微生物隔离开来。除了产生黏液层,这些肠上皮细胞构成一个连续的物理屏障,由紧密连接(tight junctions)、粘着连接(adherens junctions)以及桥粒(desmosomes)形成的上皮连接复合物构成。紧密连接的失调往往与肠道通透性增加和肠道炎症相关,例如在炎症性肠病(inflammatory bowel diseases, IBDs)患者中人们观察到上皮细胞连接完整性出现异常,暗示细胞连接的异常可能参与了与IBDs的发病机制。因此,细胞连接相关的基因表达需要被严格调控,以确保肠道上皮屏障的完整性。然而,控制肠道上皮细胞连接的转录调控机制至今未明。
以往对于肠道上皮细胞屏障功能的转录调控机制研究多集中在转录起始阶段的序列特异性转录因子功能和表观遗传学修饰等,但是对于转录起始后(如转录延伸)调控是否参与肠道上皮细胞屏障功能的维持尚不清楚。转录起始后调控尤其是转录延伸负调控因子NELF复合物参与的转录暂停过程,在多种生命过程中都起到重要作用。其中胡小玉课题组于2020年发文阐述了NELF在巨噬细胞活化过程中的动态变化及其调控巨噬细胞分泌细胞因子的关键作用(Nat Commun, 2020)。这一研究结果暗示了NELF复合物可能在肠道上皮细胞稳态维持中也发挥了重要作用,于是,课题组研究人员通过构建Nelfb基因的肠道上皮细胞特异性缺陷小鼠,研究了NELF复合物介导的转录起始后调控机制在肠道上皮细胞中的功能。
研究初期,课题组研究人员发现在稳态情况下,肠上皮NELF缺陷小鼠的肠上皮组织结构、细胞分化等未发生异常,但是在DSS构建的小鼠肠炎模型实验中,NELF缺陷小鼠相较于对照组小鼠表现出显著的体重下降和死亡率上升、以及严重的组织损伤和免疫细胞浸润等现象。随后,研究人员尝试探索NELF在缓解肠炎过程中发挥怎样的作用,利用组织免疫荧光染色和透射电子显微镜等技术,发现DSS诱导肠炎早期(第二天)时,NELF缺陷小鼠的肠道上皮细胞便出现大量类似细胞坏死性(necroptosis)死亡。然而在抗生素处理之后,死亡细胞数量明显减少,暗示NELF缺陷引起的上皮细胞死亡可能依赖于菌群刺激。进一步的细胞水平和分子水平上的探究发现,NELF缺陷小鼠在稳态条件下便出现部分上皮细胞死亡,并且是MLKL依赖的细胞坏死,而DSS作用加剧了上皮细胞的坏死。研究人员通过ChIP-seq等分子生物学手段发现,肠上皮NELF缺陷会导致大量上皮细胞特异性基因表达紊乱。值得注意的是,实验结果显示肠道上皮NELF可以通过直接靶向启动子区域调控多种细胞连接相关基因(如Cldn3、Cgn、Cldn23、Jup等)的表达,并且在敲除NELF之后,细胞连接基因在mRNA和蛋白水平上显著下调(图1)。最后结合动物体内实验和原位杂交(FISH)等技术验证了在诱导性结肠炎早期阶段,肠上皮NELF缺陷导致上皮通透性增加、共生菌入侵加剧,且肠炎发展依赖于共生菌入侵。
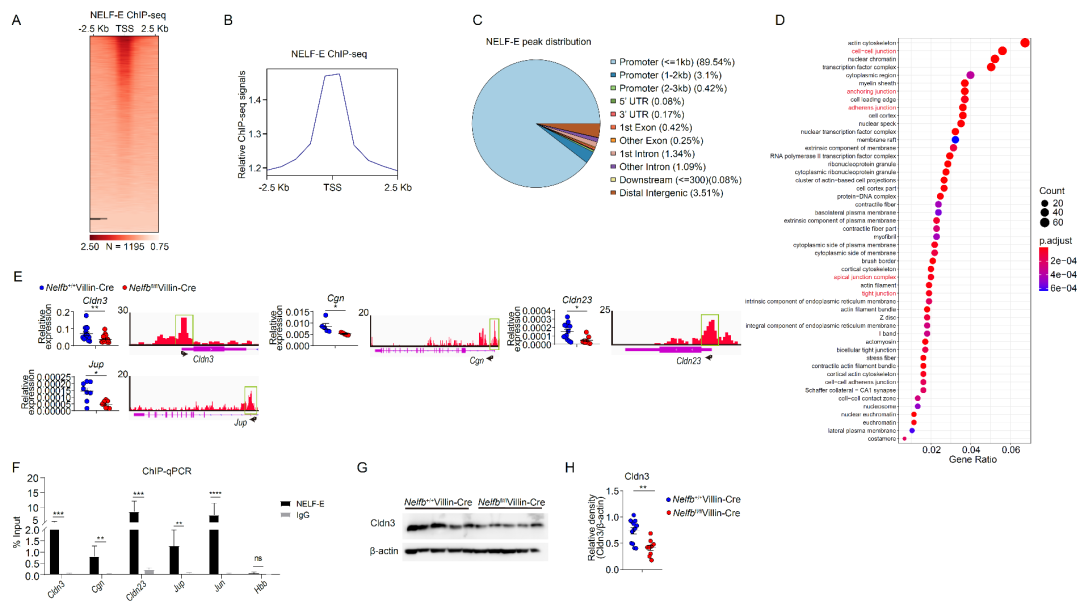
图1 . 肠上皮NELF通过直接靶向启动子区域调控多种细胞连接相关基因的表达
综合上述实验论证表明,在DSS诱导肠炎初期肠上皮NELF缺陷首先导致细胞连接相关基因显著下调,促使上皮细胞屏障功能下降,加剧共生菌入侵以及共生菌依赖的上皮细胞坏死,而细胞坏死又进一步加剧了屏障破坏,最终引起严重的炎症反应。该研究首次揭示了转录起始后阶段转录延伸调控因子NELF复合物特异性调节肠道上皮屏障功能相关基因的表达,在维持肠道屏障稳态的过程中发挥了至关重要的作用。
清华大学医学院、清华大学免疫学研究所胡小玉教授和医学院助理研究员郭雪坤博士为本文的共同通讯作者,已毕业的欧加尧博士和已出站的博后管晓星博士为该论文共同第一作者。此外,来自清华大学医学院的徐沪济教授、及其博士研究生王天娇和胡小玉课题组的博士研究生王佳丽、张彬对本研究做出了重要贡献。该研究得到了乔治·华盛顿大学李荣(Rong Li,音译)教授的重要支持。该研究得到了国家自然科学基金委、科技部、清华大学-北京大学生命科学联合中心以及清华大学免疫学研究所资助。
文章链接:
https://www.nature.com/articles/s41385-021-00465-9